Wat beïnvloedt arteriolaire weerstand en glomerulaire filtratiesnelheid?
De controle van de weerstand tegenovergesteld aan de afferente en efferente arteriolen van de renale glomerulus hangt af van talrijke factoren, zowel systemisch als lokaal.
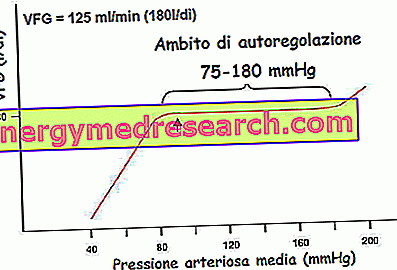
De zelfregulering van de glomerulaire filtratiesnelheid omvat verschillende intrinsieke nefronmechanismen, waaronder we herinneren aan:
- myogene respons: intrinsiek vermogen van vasculaire gladde spieren om te reageren op drukveranderingen.
Indien uitgerekt door de systemische druktoename, reageert de gladde spier van de afferente arteriolen door samentrekken; op deze manier verhoogt het de weerstand tegen de stroming door de hoeveelheid bloed die door de arteriole stroomt te verminderen en daarmee de hydrostatische druk uitgeoefend op de wanden van de glomerulaire capillairen → de filtratiesnelheid wordt verminderd.
Omgekeerd, als de systemische arteriële druk afneemt, ontspant de arteriolaire spier en expandeert het vat op een maximale manier; verhoogt dus de bloedstroom in de glomerulus en verhoogt daarmee ook de glomerulaire hydrostatische druk en de filtratiesnelheid. Er dient echter op te worden gewezen dat vasodilatatie niet zo effectief is als vasoconstrictie, omdat de afferente arteriole onder normale omstandigheden al behoorlijk verwijd is. Hierdoor kan de myogene respons goed compenseren voor de toename van de systemische arteriële druk en iets minder voor een mogelijke daling.
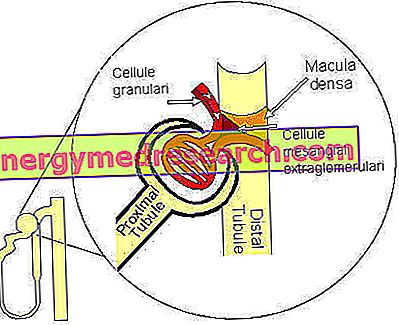
- tubulo-glomerulaire feedback: de stroomvariaties van de vloeistof die het laatste stuk van de lus van Henle passeert en het initiële kanaal van de distale tubulus beïnvloeden de glomerulaire snelheid. In de loop van Henle vinden processen van reabsorptie van water en natrium- en chloride-ionen plaats. De specifieke gevouwen structuur van de nephron zorgt ervoor dat het laatste deel van de lus van Henle tussen de afferente en efferente arteriolen naar de renale glomerulus gaat. In dit gebied tussen de twee structuren wordt een structurele en functionele relatie tot stand gebracht om een echt "apparaat" gedefinieerd "juxtaglomerulare apparaat" te vormen. Op de punten waar ze in contact komen, hebben zowel de arteriolaire wanden als die van de tubulus een gemodificeerde structuur die In het bijzonder bestaat de gemodificeerde buisvormige structuur uit een celplaat die de dichte macula wordt genoemd, terwijl de aangrenzende wand van de afferente arteriola gespecialiseerde gladde spiercellen bevat, granulaire cellen (of juxtaglomerular of JG) genoemd. ze scheiden renine uit, een proteolytisch hormoon dat betrokken is bij de hydrosaline balans, met hypertensieve effecten.
De beheersing van de weerstand van afferente en efferente arteriolen wordt ook gereguleerd door systemische factoren. Aan de andere kant is één van de belangrijkste functies van de nier het reguleren van de systemische arteriële druk, dus het is belangrijk dat de glomeruli veranderingen in de systemische arteriële druk ontvangen en dienovereenkomstig de VFG aanpassen. Deze veranderingen worden doorgegeven aan de endocriene en nieren van de nieren.
De zenuwcontrole van VFG wordt toevertrouwd aan sympathische neuronen die zowel de afferente als de efferente arteriolen innerveren. Sympathische stimulatie, gemedieerd door de afgifte van adrenaline, veroorzaakt vasoconstrictie, vooral van de afferente arteriola. Dientengevolge, bepaalt een sterke activering van het sympathische, bijvoorbeeld als gevolg van een sterke bloeding of een ernstige uitdroging, een samentrekking van de afferente en efferente arteriolen naar de glomeruli, waardoor zowel de snelheid van glomerulaire filtratie als de bloedstroom naar de nieren wordt verminderd. Op deze manier proberen we het watervolume zo hoog mogelijk te houden.
De endocriene controle van VFG is toevertrouwd aan verschillende hormonen. Naast circulerende adrenaline, waarvan de vasoconstrictieve effecten zojuist zijn beschreven, wordt arteriolaire resistentie ook verhoogd door angiotensine II. In het laatste geval beïnvloedt vasoconstrictie vooral de efferente arteriolen, zodat de toename in druk in de glomerulaire capillairen de glomerulaire filtratiesnelheid verhoogt. Onder de vasodilaterende stoffen die tegen het vasoconstrictieve effect van het sympathische zenuwstelsel en angiotensine II zijn, herinneren we aan enkele prostaglandinen (PGE2, PGI2, Bradykinin), die de weerstand tegen de aangeboden stroom verminderen, vooral van afferente arteriolen. Dit resulteert in een toename van de glomerulaire filtratiesnelheid. Stikstofmonoxide oefent ook een vaatverwijdende werking uit op arteriolair niveau.
De endocriene actie vindt plaats op het niveau van de podocyten of mesangiale cellen. De samentrekking of ontspanning van de laatste, waarvan we ons herinneren dat deze in de ruimten rond de haarvaten van de nierglomeruli is geplaatst, wijzigt het oppervlak van het capillaire oppervlak dat beschikbaar is voor filtratie. De podocyten veranderen de grootte van de glomerulaire filtratiescheuren; als deze breder worden, neemt het filtratieoppervlak toe, daarom wordt ook de glomerulaire filtratiesnelheid verhoogd.
Bekijk de video
X Bekijk de video op youtube





